- L'ANMV
- Nos métiers
- Mes démarches
- Je suis un industriel
- Médicaments vétérinaires
- Déposer un dossier électronique sur CESP
- Demander une autorisation de médicament
- Demander une autorisation d'essai clinique
- Demander une autorisation d'importation
- Demander une autorisation de commerce parallèle
- Demander une autorisation d'exportation
- Demander une libération officielle de lots
- Demander une libération exceptionnelle de lots
- Demander une dérogation pour la préparation d'un autovaccin
- Demander un transfert d'AMM
- Déclarer un code GTIN
- Établissements et inspection
- Déposer une demande sur la plateforme CESP
- Demander une inspection
- Demander une autorisation d'ouverture
- Demander une modification d'autorisation d'ouverture
- Déposer un état annuel
- Déclarer une personne responsable (expérimentation animale)
- Demander un changement administratif
- Demander un transfert d'autorisation d'ouverture
- Demande relative aux autovaccins
- Surveillance du marché
- Antibiorésistance
- Taxes et redevances
- Médicaments vétérinaires
- Je suis un vétérinaire ou un pharmacien
- Autres
- Je suis un industriel
- Nos dossiers
- Europe & International
- Europe
- International
- Organisation mondiale de la santé animale (OMSA)
- Harmonisation internationale des exigences techniques pour l’enregistrement des médicaments vétérinaires (VICH)
- Pharmaceutical inspection cooperation scheme (PICs)
- Organisation de développement et de coopération économique (OCDE)
- Codex alimentarius
- Accords de coopération
- Modules e-learning
- S'abonner à notre newsletter
Portail Médicaments vétérinaires
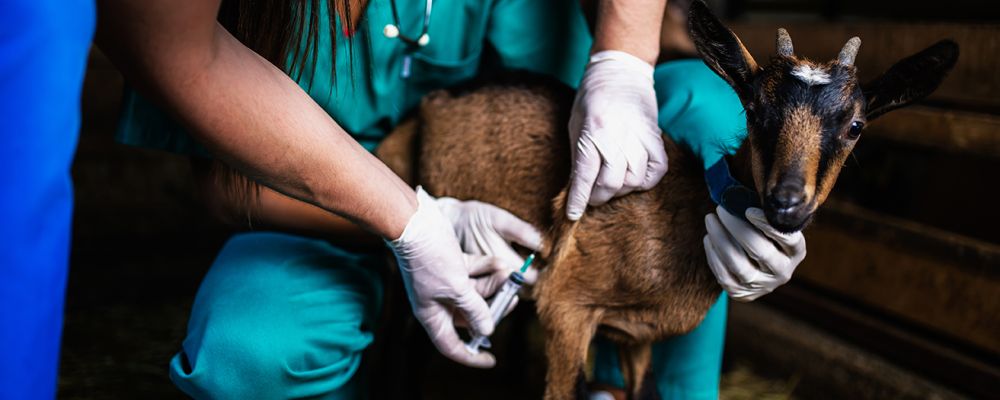
Contrôle de la qualité des médicaments et falsification
Chaque année, au sein de son laboratoire, l’Unité Surveillance du Marché et de Pharmacovigilance de l’ANMV contrôle une série de médicaments vétérinaires commercialisés en France.
La sélection des médicaments inclus dans le programme annuel du laboratoire est issue d’une analyse de risques. Celle-ci s’inspire du modèle de cotation des médicaments initié au niveau européen. Cette programmation prend en compte également le suivi de non conformités précédemment détectées, les médicaments ayant fait l’objet de défauts qualité les années précédentes, les demandes d’autres départements de l’agence.
Ces contrôles permettent de vérifier le respect des spécifications déclarées dans l’Autorisation de Mise sur Marché.
Des difficultés d’utilisation des médicaments observées sur le terrain (solubilité, remise en suspension…) peuvent également être testées en condition de laboratoire.
Le laboratoire a la capacité analytique de confirmer d’éventuelles falsifications de médicaments vétérinaires.
Les médicaments contrôlés peuvent avoir des AMM nationales ou européennes. Lorsqu’il s’agit d’AMM européennes, les programmes font l’objet de coordination au niveau de la Direction Européenne de la Qualité des Médicaments et Soins de Santé du Conseil de l’Europe. L'EDQM est en charge de la Pharmacopée Européenne, le référentiel en matière de qualité des médicaments qu’ils soient à usage humain ou vétérinaire. Elle coordonne aussi le réseau des Laboratoires Officiels de Contrôle des Médicaments (OMCL). Le laboratoire de l'ANMV, au sein de l'USMP, est reconnu membre à part entière de ce réseau. Le maintien de ce statut est assuré par des audits réguliers de reconnaissance par les pairs (ou à défaut via les audits d'accréditation nationale) du système de Management de la Qualité selon le référentiel ISO 17025.
Pour accéder aux dossiers de la thématique
Pour toute question relative au contrôle de la qualité des médicaments, vous pouvez contacter le laboratoire de l'Agence à l'adresse suivante : ucqm@anses.fr